某化学实验小组为了验证SO 2 和Cl 2 的漂白性,设计了如下图所示的实验装置。请回答下列问题:
某化学实验小组为了验证SO 2 和Cl 2 的漂白性,设计了如下图所示的实验装置。请回答下列问题: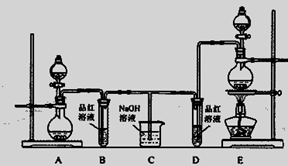 (1)他们制备SO 2 和Cl 2 所依据的原理分别是:Na 2 SO 3 +H 2 SO 4 =Na 2 SO 4 +H 2 O+SO 2 ↑、MnO 2 +4HCl(浓)  MnCl 2 +Cl 2 ↑+2H 2 O,则上图A、E装置中用来制Cl 2 的装置是 MnCl 2 +Cl 2 ↑+2H 2 O,则上图A、E装置中用来制Cl 2 的装置是 (填序号),反应中盐酸所表现的性质是 ; (2)反应开始后,发现B、D试管中的品红溶液都褪色,停止通气后,给B、D两个试管中的溶液加热,B试管中的现象是 ; (3)装置C的作用是 ; (4)NaOH(足量)溶液分别与两种气体反应的离子方程式是 、 ; (5)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色。查阅资料得知:两种气体按体积比1∶1混合,再与水反应可生成两种常见酸,因而失去漂白作用。该反应的化学方程式为 。 |
-
2024-08-141个回答
-
把数38490按四舍五入精确法取近似值精确到千位是 ___ .
2024-08-141个回答
-
2024-08-141个回答
-
2024-08-141个回答
-
特别难的数学题1265330000精确到千万位,并用科学计数法表示为---------.这个近似数的有效数字有-----
2024-08-144个回答
-
2024-08-143个回答
-
2024-08-143个回答
-
2024-08-142个回答
-
4200万精确到百万位并用科学计数法表示 老师说答案是4.20*10^3万 ,问过程?我认为是4.2*10^3
2024-08-141个回答
-
把数精确到千位用科学计数法么?有一道题是这样的:把64497精确到千位可记为()A.6.4*10的四次方 B.64000
2024-08-142个回答
-
(20分)如图所示,A、B两个小物体(可看成质点)的质量分别为2m、m,它们栓接在跨过定滑轮的细绳两端,细绳不可伸长,且
2024-08-141个回答
-
不论m为何实数,直线(m-1)x-y+2m+1=0恒过定点( )
2024-08-141个回答
-
已知方程(3m-4)X的平方-(5-3m)x-4m=-2m是关于x的一元一次方程,(1)求m和x的值.
2024-08-141个回答
-
已知函数f(x)=x2-4x+a+3,g(x)=mx+5-2m.
2024-08-141个回答
-
2024-08-143个回答
-
解答这几题100分,要过程.一.1.24平方米=( )升=( )毫升二.把7分之2M分成8分,每分占总数的( )%,甲数
2024-08-145个回答
-
函数f(x)=2sinx.cosx + 2m cos²x 若m<0 求f(x) 在闭区间 0到二分之π 上的最
2024-08-145个回答
-
初一寓言作文,600~400字的,最好不和别人重复.明天就交老师了.最好是动物的.
2024-08-141个回答
-
小学英语作文我最喜欢的动物是小兔子,它长着两只长耳朵,兔子喜欢吃萝卜,白菜,它蹦蹦跳跳很可爱,所以我很喜欢它.
2024-08-145个回答
-
2024-08-141个回答
你能帮帮他们吗
-
若f(a)=(3m-1)a+b-2m,当m∈[0,1]时f(a)≤1恒成立,则a+b的最大值为( )A. [1/3]
2024-08-142个回答
-
2024-08-141个回答
-
人和动物的故事作文600字好写好!或者可以写 动物的故事!写兔子的!
2024-08-141个回答
-
2024-08-141个回答
-
2024-08-144个回答
精彩回答
-
2024-08-146个回答
-
知道圆柱高度和直径怎么算容积有一个圆柱体,高50厘米,直径是130CM,怎么计算出它里面有多少沙子,
2024-08-146个回答
-
2024-08-142个回答
-
某车间生产一批零件,495个合格,合格率是99%,一共生产了( )零件
2024-08-146个回答
-
假如你是王平,你的一位美国网友Mary在你过生日时寄给你一个MP5播放器作为礼物,为此你写信向她表示感谢.信中要包含以下
2024-08-143个回答
